Vaksin Bivalen Berbasis Rvsv Terhadap Varian Delta SARS-Cov-2 dan Influenza
Dalam penelitian terbaru yang dipublikasikan di server pracetak bioRxiv*, para peneliti mengembangkan empat recombinant vesicular stomatitis virus (rVSV)-based bivalent vaccines yang berbeda terhadap severe acute respiratory syndrome coronavirus 2 (SARS-CoV-2) dan virus influenza.
Latar belakang
Sejak SARS-CoV-2 pertama kali diidentifikasi pada akhir
2019, beberapa strain mutan dari virus ini telah muncul. Di antaranya termasuk
varian SARS-CoV-2 variants of concern (VOCs), yang dianggap sebagai jenis virus
yang paling mudah menular dan mematikan.
SARS-CoV-2 Delta VOC (B.1.617.2), yang pertama kali
diidentifikasi di India pada Desember 2020, dengan cepat menyebar ke seluruh
dunia dan menjadi strain SARS-CoV-2 yang beredar. Faktanya, satu penelitian
baru-baru ini menemukan bahwa individu yang terinfeksi varian Delta SARS-CoV-2
memiliki viral load yang lebih dari 1.000 kali lebih tinggi dibandingkan dengan
individu yang terinfeksi dengan strain SARS-CoV-2 asli, sehingga menjadikan
varian ini strain SARS-CoV-2 yang paling menular hingga saat ini.
Selain SARS-CoV-2, virus influenza juga sangat menular dan
terus menjadi ancaman signifikan bagi kesehatan masyarakat setiap tahun. Karena
kedua virus ini dapat ditularkan pada tingkat tinggi selama musim yang sama,
penting untuk mengembangkan vaksin multivalen yang secara bersamaan dapat
melindungi individu yang diimunisasi terhadap penyakit coronavirus 2019
(COVID-19) dan influenza.
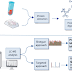
Construction and rescue of rVSV Delta SP and influenza M2e
bivalent vaccines. A) Schematic diagram of the Delta SPΔC and EboGPΔM-tM2e
immunogens present in the bivalent vaccines. a. SARS-CoV-2 Delta-SPΔCA742
(SPΔC1), containing a C-terminal 17 aa (DEDDSEPVLKGVKLHYT) deletion and a I742A
mutation as indicated. The nine mutations in Delta SP are listed in lower part.
b. Delta SPΔC2, containing the C-terminal 17 aa deletion and another 381 aa
(encompassing aa744 to aa1124) deletion in S2 domain. The eight mutations in
SPΔC2, are listed in lower part. c. EboGPΔM-RBD, the RBD of SARS-CoV-2 was used
to replace the MLD domain in EboGP. d. EboGPΔM-tM2e, four copies of influenza
virus M2 ectodomain (24 aa) polypeptide (tM2e) replaced the MLD domain in
EboGP. B) The attenuated virus entry of SPΔC1. A549ACE2 cells were infected
with equal amounts of SPΔCDelta-PVs or SPΔC1-PVs (adjusted by P24) carrying
Gaussia luciferase (Gluc) gene, as indicated. At 48hrs after infection, the
Gluc activity in the supernatant of different infected cultures was measured.
Data represent Mean ±SD of two replicates from a representative experiment out
of three performed. C and D) The attenuated cell-to-cell fusion ability of
SPΔCDelta- or SPΔC1-mediated syncytia formation was analyzed by co-culturing
the SPΔCDelta- or SPΔC1-expressing 293T cells with A549ACE2 cells. The amounts
of syncytia were counted after 24 hrs in 5 different views of microscope (C),
and were also imaged under bright-field microscopy (D). E) Schematic diagram of
VSV-EM2e/SPΔC1, VSV-EM2e/SPΔC2 and VSV-EM2e/ERBD and the virus rescuing
procedures. 293T and Vero E6 co-culture cells were co-transfected with
VSV-ΔG-EM2/SPΔC1, VSV-ΔG-EM2/SPΔC or VSV-ΔG-EM2/RBD, and helping plasmids (T7,
N, L, P plasmids). The supernatants containing V-EM2e/SPΔC1, V-EM2e/SPΔC2 and
V-EM2e/ERBD viruses were used to infect Vero E6 cells to generate the rVSV
stocks.
Tentang studi
Dalam studi saat ini, para peneliti menghasilkan tiga
kandidat vaksin rVSV replikasi yang dilemahkan. Vaksin berbasis rVSV ini
bersama-sama mengekspresikan spike protein (SP) varian Delta SARS-CoV-2 Delta
atau receptor-binding domain (RBD), serta empat salinan M2 ectodomain (M2e)
influenza A yang sangat terkonservasi yang memiliki telah menyatu dengan domain
penargetan / aktivasi DC yang berasal dari Ebola virus glycoprotein (EBOV GP).
Para peneliti menggunakan platform vaksin berbasis VSV
sebagai hasil dari kemampuannya untuk menginduksi kekebalan yang cepat dan kuat
terhadap antigen virus setelah imunisasi tunggal. Selanjutnya, kandidat vaksin
VSV sebelumnya telah berhasil dan secara bersamaan melindungi individu yang
diimunisasi terhadap beberapa patogen termasuk virus Ebola, Zika, Nipah, dan
human immunodeficiency.
Temuan studi
Vaksin rVSV bivalen yang dibuat dalam penelitian ini secara
bersamaan mengekspresikan EboGPΔM-M2e fusion protein (EM2e) EboGPΔM-SARS-CoV2
RBD fusion protein (ERBD), a full-length SPΔCDelta (SPΔC1), atau S2-deleted
SPΔCDelta (SPΔC2). Secara bersama-sama, total empat kandidat vaksin yang
berbeda dinilai dalam penelitian ini.
Untuk menyelidiki profil keamanan kandidat vaksin, para
peneliti melakukan kinetika replikasi vaksin berbasis rVSV di berbagai lini sel
dan membandingkan hasil ini dengan sel yang diobati dengan rVSV yang mengekspresikan
VSV-G. Eksperimen ini menunjukkan bahwa vaksin berbasis rVSV tidak menargetkan
sel T CD4+, yang penting karena perannya dalam melindungi sistem kekebalan dari
serangan. Selanjutnya, kandidat vaksin rVSV ditemukan telah mengurangi
kemampuan replikasi selama percobaan in vitro ini, sehingga menunjukkan efek
sitopatik yang dapat diabaikan dalam sel.
Untuk mengevaluasi kemampuan kandidat vaksin ini untuk
menginduksi respons imun spesifik terhadap virus SARS-CoV-2 dan influenza, para
peneliti mengimunisasi tikus Balb/c dengan masing-masing vaksin bivalen VSV
secara intramuskular (IM) atau intranasal (IN) pada Hari 0 dan Hari 14.
Studi kinetika replikasi menunjukkan bahwa replikasi virus
rVSV ini secara signifikan dilemahkan dibandingkan dengan VSV tipe liar dan
tidak dapat menginfeksi limfosit T CD4+, sehingga menunjukkan karakteristik
yang sangat dilemahkan dari vaksin berbasis rVSV ini. Selain itu, studi
imunisasi dan analisis penetralan mengungkapkan bahwa serum dari tikus yang
diimunisasi V-EM2e/SPΔC1- dan V-EM2e/SPΔC2 menunjukkan aktivitas penetralan
yang secara signifikan lebih tinggi terhadap infeksi SARS-CoV-2 SPDelta-PV
daripada terhadap infeksi SPWT-PV.
Anti-SARS-CoV-2 RBD and anti-influenza M2e immune responses
induced by immunization with different bivalent VSV vaccine candidates. A)
Schematic of the bivalent rVSV vaccine candidates immunization protocol in
mouse. Balb/c mice were immunized with V-EM2e/SPΔC1, V-EM2e/SPΔC2 or
V-EM2e/ERBD via intramuscular (IM) or intranasal (IN) routes, as indicated. The
mice sera were collected at day 13 and 28 and were measured for anti-SARS-CoV-2
RBD IgG and IgA antibody levels (B-D) or measured for anti-M2e IgG and IgA
antibody levels (F-H). E, D) The anti-SARS-CoV-2 RBD and anti-M2e IgA antibody
levels at 28 day. Data represent Mean ±SD. Statistical significance was
determined using unpaired T-test. *, P < 0.05; **, P < 0.01; ***, P <
0.001; ****, P < 0.0001.
Semua kandidat vaksin juga berhasil menginduksi respon imun
spesifik influenza yang signifikan. Faktanya, kandidat vaksin utama V-EM2/SPΔC1
ketika diberikan baik IM atau IN, secara efektif melindungi tikus dari infeksi
virus influenza H1N1 yang mematikan.
Pemberian IM V-EM2e/SPΔC1 atau V-EM2e/SPΔC2 menginduksi
titer antibodi penetralisir yang lebih tinggi dan respons imun seluler yang
lebih kuat dibandingkan dengan saat vaksin ini diberikan IN. Namun, dosis
vaksin VSV yang digunakan untuk pemberian IN adalah 1.000 kali lipat lebih
rendah daripada untuk pemberian IM, sehingga menunjukkan kemungkinan kebutuhan
untuk meningkatkan dosis vaksin ini untuk mencapai respon imun yang lebih kuat
ketika diberikan IN.
Para peneliti mengamati respons sel T yang kuat yang
dicirikan oleh tingginya tingkat sitokin yang disekresikan termasuk interferon
(IFN)-γ dan interleukin (IL)-4 dalam splenosit dari tikus yang distimulasi
dengan kandidat vaksin berbasis rVSV. Perbedaan signifikan dalam rasio sitokin
Th1-sitokin/Th2-sitokin (IFN-γ/IL-5) diamati antara sampel yang diisolasi dari
tikus yang diimunisasi IM dan IN. Ini menunjukkan bahwa imunisasi IM memicu
respons seluler yang bias Th1 tetapi relatif seimbang Th1/Th2, sementara
imunisasi IN memicu respons seluler yang sangat bias Th1.
Ada kemungkinan kuat bahwa respons Th2 terkait dengan antibody-dependent
enhancement (ADE) infeksi pada tikus yang divaksinasi dengan vaksin yang tidak
aktif dan ditantang oleh SARS-CoV-1. Namun, para peneliti menunjukkan bahwa
respons seluler bias Th1 yang diamati kemungkinan disebabkan oleh pemberian IM
dan IN dari vaksin SARS-CoV-2 berbasis rVSV.
Kesimpulan
Temuan penelitian saat ini menunjukkan bahwa vaksin berbasis
rVSV yang dijelaskan di sini, terutama kandidat vaksin utama V-EM2e/SPΔC1,
dapat menghasilkan antibodi penetralisir tingkat tinggi terhadap strain Delta
SARS-CoV-2, serta H1N1. dan virus influenza H3N2. Penyelidikan lebih lanjut
diperlukan untuk mengkonfirmasi kemanjuran kandidat vaksin ini terhadap varian
Delta SARS-CoV-2 dan strain influenza pada model hewan yang lebih tinggi,
terutama primata non-manusia sebelum kandidat vaksin ini dapat diuji pada
manusia.
“Fitur unik yang penting dari platform vaksin dalam
penelitian ini adalah dapat secara bersamaan melindungi terhadap virus
SARS-CoV-2 dan influenza.”
*Pemberitahuan Penting
bioRxiv menerbitkan laporan ilmiah awal yang tidak ditinjau
oleh rekan sejawat dan, oleh karena itu, tidak boleh dianggap sebagai
konklusif, memandu praktik klinis/perilaku yang berhubungan dengan kesehatan,
atau diperlakukan sebagai informasi yang mapan.
Journal reference:
Ao, Z., Ouyang, M. J., Olukitibi, T. A., et al. (2021).
Development and Characterization of Recombinant Vesicular Stomatitis Virus
(rVSV)-based Bivalent Vaccine Against COVID-19 Delta Variant and Influenza
Virus. bioRxiv. doi:10.1101/2021.12.14.472657.
https://www.biorxiv.org/content/10.1101/2021.12.14.472657v1.









No comments